IBS 유전체교정연구단, '크리스퍼 유전자가위' 정확성 입증…유전질환 치료제 개발 활용 기대
"질병 원인이 되는 유전자를 미리 잘라버릴 순 없을까". 이 같은 상상이 현실로 구현될 것으로 보인다.
기초과학연구원(IBS) 유전체교정연구단은 서울대 의대(김종일 교수), 툴젠과의 공동연구를 통해 유전체 교정 도구인 '크리스퍼(CRISPR) 유전자가위'가 인간세포 내에서 정확히 표적 유전자에만 작용할 수 있음을 입증했다고 10일 밝혔다.
크리스퍼 유전자가위는 인간 및 동식물 세포에서 특정 유전자의 염기서열 DNA를 절단해 유전체 교정을 가능하게 하는 인공 제한효소이다.
이번 연구로 보다 정교한 유전체 교정이 가능해져 유전질환 치료 및 항암 세포치료제 개발에 활용을 기대해 볼 수 있게 됐다.
크리스퍼 유전자가위는 줄기세포 및 체세포에서 유전병의 원인이 되는 돌연변이를 교정하거나 항암 세포치료제를 개발하는 도구가 될 것으로 큰 기대를 모으고 있다.
하지만 크리스퍼 유전자가위 활용시 원하는 유전자를 정확히 제거할 수 있는지를 측정할 방법이 없어 '안전성 문제'가 줄곧 제기돼 왔다. 크리스퍼 유전자가위가 표적 유전자의 염기서열과 유사한 '비표적 염기서열'에도 변이를 일으킬 수 있었기 때문이다.
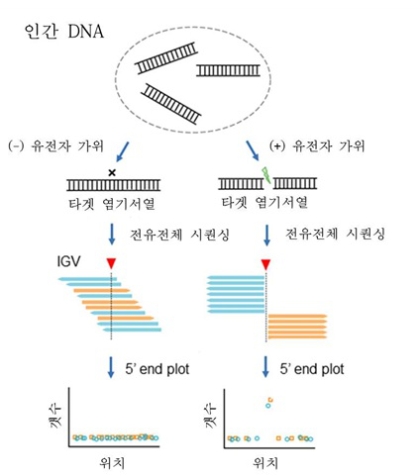
연구진은 인간의 DNA를 크리스퍼 유전자가위로 처리한 후 유전체 시퀀싱을 통해 크리스퍼 유전자가위에 의해 잘리는 표적 염기서열과 비표적 염기서열을 찾는 방법을 개발했다.
또 크리스퍼 유전자가위를 구성하는 가이드 RNA의 말단에 ‘구아닌(G) 염기’를 추가함으로서 인간 유전체에서 단 한 군데에만 작용하는 정교한 유전자가위를 만드는 데 성공했다.

김진수 IBS 유전체교정연구단장은 "만약 크리스퍼 유전자가위가 의도하지 않은 DNA 염기서열을 자르게 되면 원하지 않는 돌연변이를 유발할 수 있다"며 "크리스퍼 유전자가위의 안전성을 확인할 수 있어 유전자치료제, 세포치료제 개발에 큰 진전이 있을 것"이라고 말했다.
이번 연구 결과는 생명과학 및 화학 분야 세계 최고권위의 저널인 네이처 메소드(Nature Methods)지에 10일 발표됐다.
또 이 기술은 지난달 네이처 메소드가 선정한 '2015년 기대되는 중요 실험기법' 8개 중 하나로 소개돼 주목을 이끈 바 있다.
독자들의 PICK!
◆용어설명
▶유전체 시퀀싱=A, C, G, T 네 종류의 염기로 구성된 생명체 DNA 염기서열 순서를 규명하는 기법이다. 인간 유전체는 30억 쌍의 염기로 구성돼 있다.
