김진수 IBS 유전체 교정연구단장 주도…유전질환·항암 세포치료제 개발 활용 기대
새로운 절단효소를 장착한 신형 유전자가위인 ‘크리스퍼 Cpf1’(CRISPR Cpf1)의 정확한 성능이 처음으로 입증됐다.
기초과학연구원(IBS) 유전체 교정연구단 김진수 연구단장팀은 크리스퍼 Cpf1이 기존 크리스퍼 Cas9에 비해 유전자 교정 정확성이 뛰어나다는 사실을 자체 개발한 실험방법으로 7일 밝혔다. 신형 유전자가위의 성능이 확인됨에 따라 3세대 유전자가위의 세대교체가 이뤄질지 관심이 모아지고 있다.
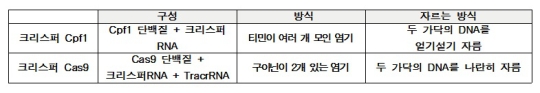
최근 과학계에서 가장 많이 활용되는 유전자가위는 크리스퍼 Cas9이다. Cas9은 특정 DNA 염기를 잘라내는 효소이름이다. Cas9 대신 Cpf1이라는 새로운 효소가 지난해 처음 개발됐다.
Cpf1 단백질은 지난해 MIT의 펑장(Feng Zhang) 교수가 Cas9을 대신할 절단효소를 찾던 중 발견해 학계에 보고한 절단효소다. 문제는 이 효소가 표적 위치를 정확히 자르는지, 비표적 위치에서 오작동하지는 않는지가 전혀 알려져 있지 않다는 점이다.
김진수 단장팀은 자체 개발한 ‘절단 유전체 시퀀싱’((Digenome-seq) 기법으로 세계에서 처음으로 크리스퍼 Cpf1 유전자가위가 비표적 위치에서 오작동할 확률을 측정, 그 정확성을 규명했다.
절단 유전체 시퀀싱 기법은 유전자가위 처리 전과 후를 한 눈에 파악해 잘린 위치를 구별하는 방식이다. 인간 세포에서 분리 정제한 유전체 DNA를 크리스퍼 Cpf1으로 처리한 뒤, 전체 시퀀싱을 하고 잘려진 표적 염기서열과 비표적 염기서열을 비교한다.
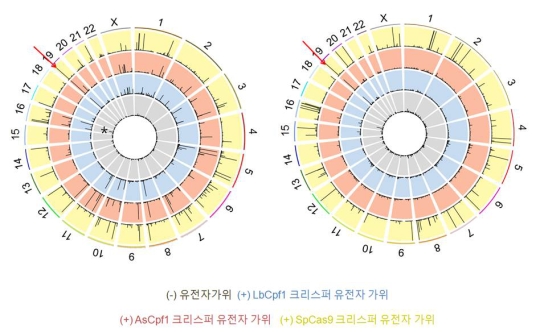
연구진은 이 기술로 크리스퍼 Cpf1의 정확성을 측정한 결과, 비표적 위치를 절단한 경우가 크리스퍼 Cas9에 비해 현저히 적은 것을 확인했다. 심지어 인간 유전체 DNA 32억개 염기서열 중 표적 위치만 정확히 자르고 비표적 위치는 단 한 군데도 자르지 않는 경우도 있었다. 즉, 원치 않는 부위를 자르는 경우가 없을 정도의 수준이다. 이는 크리스퍼 Cpf1이 오작동할 확률이 매우 낮다는 의미로 크리스퍼 Cas9에 비해 높은 정확성을 보였다고 할 수 있다.

또 연구단은 여러 표적 위치에 대해 각각 크리스퍼 Cpf1의 정확성을 측정한 결과, 경우에 따라 몇 개의 비표적 위치를 자르는 것도 있었으나 이 또한 Cpf1 단백질과 크리스퍼 RNA를 혼합한 형태를 직접 세포에 전달하는 방식으로 정확도를 향상시켜 표적 위치만 자를 수 있음을 입증했다.
독자들의 PICK!
김진수 단장은 “크리스퍼 Cpf1을 이용해 유전질환의 원인이 되는 돌연변이를 교정하거나 부작용 없는 항암세포 치료제를 개발할 수 있다”며 “향후 이 기술은 유전자 및 줄기세포 치료제 개발, 고부가가치 농축산물 품종 개량 등에서 널리 활용될 것”으로 기대했다.
이번 연구성과는 국제학술지인 ‘네이처 바이오테크놀로지’ 7일자 온라인판에 게재됐다.
