전기에너지를 빛에너지로 전환..파장 따라 다른 색 구현
LED는 전압을 가하면 빛을 발해 '빛의 반도체'로 불린다. 전기에너지를 빛 에너지로 변환시키는 반도체다.
이와는 반대로 태양으로부터 받은 빛에너지를 전기에너지로 바꿔주는 이극반도체(다이오드)는 포토다이오드라고 불리며 이는 태양전지에 자주 활용된다.
LED가 빛을 낼 수 있는 것은 LED가 양(+)과 음(-)의 전기적 성질을 지닌 2개 이상의 화합물로 구성돼 있기 때문이다.
LED는 통상적으로 주기율표상의 3족과 5족 원소를 조합해 만든다. 4족이 4개의 전자를 가져 가장 안정적인 가운데 3족은 4족에 비해 전자가 하나 적고 그 자리는 정공(Hole)이 차지하고 있다. 5족은 4족보다 전자를 하나 더 갖고 있다.
3족 원소처럼 정공이 하나 있는 것은 P(Positive)형 반도체, 5족 원소처럼 전자가 하나 많은 것은 N(Negative)형 반도체로 불러 LED를 'P-N형 반도체'의 결합이라고도 부른다.
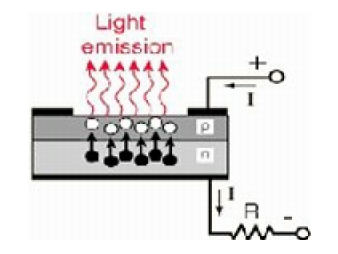
이런 화합물에 전압을 걸어주면 N층의 남는 전자가 P층의 정공으로 이동, 결합하면서 에너지를 발산한다. 이 에너지는 주로 열이나 빛의 형태로 방출되는데 빛으로 발산되는 게 LED다.
LED가 빛을 내는 발광 원리를 쉽게 이해하려면 널뛰기와 비교할 수 있다.
명절 때 하는 널뛰기처럼 한쪽에서 먼저 힘을 가하면 반대쪽 사람이 그 힘에 의해 공중으로 올라가면서 불안정한 상태가 되고, 그 사람이 중력에 의해 안정을 되찾기 위해 제자리로 돌아오면서 자신에게 가해졌던 힘과 같은 힘을 반대쪽 사람에게 전달하는 형태가 된다.
널뛰기는 이 때 위치에너지가 동일한 위치에너지로 바뀌지만 LED에서는 위치에너지가 빛에너지 형태로 외부로 방출되는 것이 다르다. 물리학에서는 에너지보존의 법칙에 따라 위치에너지만큼의 동일한 에너지가 나오는데 이것이 빛일 수도 있고 열일 수도 있다.
LED를 만드는데 쓰이는 대표적인 화합물로는 갈륨 아세나이드(GaAs), 갈륨 아세나이드 포스파이드(GaAsP), 갈륨 포스파이드(GaP), 갈륨 나이트라이드(GaN) 등이 있다.
독자들의 PICK!
화합물의 종류가 LED의 색상도 결정한다. 파장이 짧은 인듐갈륨나이트라이드(InGaN)의 경우 청색 계열, 파장이 긴 알루미늄갈륨아세나이드는 적색의 빛을 낸다.
일반 조명과 같은 흰 빛을 내는 백색(White) LED를 만드는 방법은 크게 3가지로 분류할 수 있다. 빛의 3원색인 △적색, 녹색, 청색 LED를 조합하거나 △청색 LED에 황색 형광체를 도포하거나 △UV(자외선) LED에 적·녹·청 3색 형광체를 사용하는 방식이다.
현재 상용화된 백색 LED는 대부분 청색 LED에 황색 형광체를 씌우는 방식으로 만들어진다.
LED가 처음 발견된 것은 1923년. 당시 반도체 소재인 실리콘카바이드(SiC)에 직류 전류를 흘려 발광된 물질이 최초의 LED로 알려져 있다.
실용적인 최초의 LED는 1962년 미국 제너럴일렉트릭(GE)이 GaAsP 화합물을 이용해 개발한 LED이며 1968년 미 몬산토사가 본격 양산하기 시작했다.
이후 1986년 일본의 아카사키 교수가 질화물(나이트라이드)계 반도체를 처음 소개했고 이듬해 일본 니치아화학공업의 슈지 나카무라 박사가 청색 LED를 최초로 개발했다.
니치아는 이어 1997년 청색 LED에 황색 형광체를 도포해 단일 칩으로는 최초의 백색 LED를 구현했다.