한화케미칼 엔브렐 항체시밀러 식약청에 허가 신청
우리나라에서셀트리온(212,500원 ▲1,000 +0.47%)'램시마'에 이어 세계2호 항체 바이오시밀러(바이오복제약)탄생이 임박했다.
6일 관련업계와 식약청에 따르면 최근한화케미칼(51,800원 ▲7,400 +16.67%)은 엔브렐의 바이오시밀러 'HD203'에 대한 국내 임상1상과 3상 시험을 모두 마무리하고 식약청에 품목허가를 신청했다.
엔브렐은 미국 와이어스사의 항체 류마티스 관절염 치료제로 지난해 전 세계 매출은 79억달러 수준이다. 'HD203'은 엔브렐과 동일한 효과를 나타내는 바이오시밀러로 세포주 개발부터 배양, 정제, 제형화에 이르기까지 모두 한화케미칼에서 개발했다. 이 회사는 'HD203'에 대한 국내 임상1상 시험과 3상 시험을 마쳤다.
셀트리온이 앞서 지난 7월 품목허가를 받고 이달 국내서 시판에 들어간'램시마'도 류머티스 관절염 항체 바이오시밀러다. 램시마의 오리지널은 미국 존슨앤존슨가 생산하는 레미케이드다.
식약청은 HD203의 안전성·유효성 심사와 생산시설 실사를 거처 허가 여부를 결정할 예정이다. 이르면 올해 말께 허가가 예상된다.
한화케미칼은 이미 지난해에 미국 MSD사와 'HD203'에 대한 글로벌 판매계약을 체결했다. 계약기간은 2015년부터 2024년까지며 전체 계약금액은 7억2000만 달러다. 또 오송생명과학단지에 7000리터급 생산시설을 건설하고 있다.
류마티스관절염 항체바이오의약품 시장은 2010년 237억달러 시장을 형성하고 있고 연평균 8.3%씩 성장해 2016년 381억달러 시장을 형성할 것으로 전망되고 있다. 이중 레미케이드, 엔브렐 그리고 애보트의 휴미라 처럼 TNF-α를 타깃으로 하는 항체바이오의약품의 비중이 90%가 넘는다.
이승호 우리투자증권 연구원은 "레미케이드, 엔브렐, 휴미라는 류머티즘 관절염 1차 표준 치료제로서의 입지가 명확하다"며 "안전성과 유효성, 약물경제성, 편의성이 우수해 시장성 축소 가능성은 적다"고 분석했다. 그는 "바이오시밀러는 기존 바이오의약품 대비 저렴한 약가가 장점"이라며 "가격에 민감한 신흥국에서 시장을 형성할 수 있을 것"이라고 전망했다.
특히 램시마에 엔브렐 바이오시밀러까지 국내 시장에 나올 경우 저렴한 항체 류마티스관절염치료제 시장이 커질 가능성도 있다는 평가다.
독자들의 PICK!
다만 지난해 류마티스관절염 항체치료제 국내 시장규모는 620억원 수준에 불과하다. 따라서 셀트리온과 한화케미칼의 항체 바이오시밀러가 성과를 거두기 위해서는 해외시장 진출에 반드시 성공해야할 것으로 보인다.
셀트리온은 글로벌임상시험을 마치고 유럽의약품청(EMA)에 램시마의 허가를 신청해 놓은 상태다. 반면 한화케미칼이 해외에 진출하기 위해서는 글로벌 임상시험을 다시 진행해야 한다.
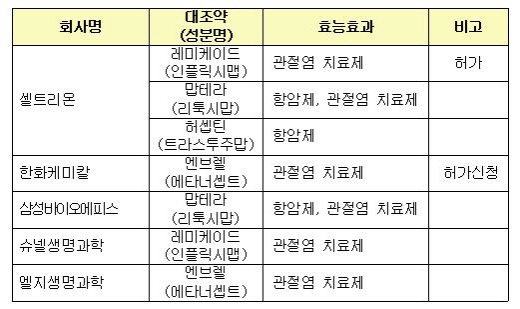
[국내 주요 바이오시밀러 임상시험 승인 현황]