[이 기사에 나온 스타트업에 대한 보다 다양한 기업정보는 유니콘팩토리 빅데이터 플랫폼 '데이터랩'에서 볼 수 있습니다.]
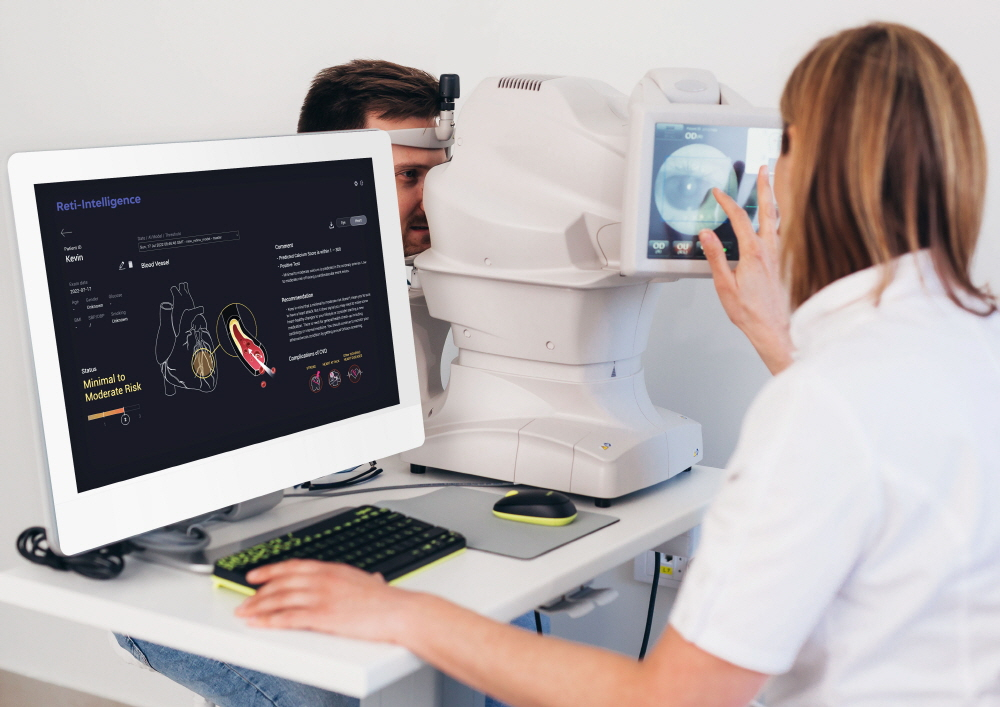
의료 AI(인공지능) 기업 메디웨일이 망막 AI 솔루션 '닥터눈'(DrNoon)에 대한 유럽 의료기기 규정 CE MDR(Medical Device Regulation) 인증을 획득했다고 6일 밝혔다.
CE MDR은 유럽 시장에서 의료기기를 판매하기 위해 충족해야 하는 의료기기 규정이다. 기존 의료기기 지침인 MDD(Medical Device Directive)를 대체해 2021년부터 시행됐다. 제품 안전성, 임상 근거, 품질관리 체계, 사후 감시 등에 대한 요구 수준을 한층 강화했다.
닥터눈은 망막 이미지를 분석해 안질환 진단을 보조하고 심혈관질환 위험을 심장 CT와 유사한 정확도로 예측하는 AI 의료기기다. 국내에서 유통 중인 안질환 진단보조 소프트웨어 '닥터눈 펀더스'와 심혈관질환 위험 평가 소프트웨어 '닥터눈 CVD'를 하나로 통합했다.
메디웨일은 이번 CE MDR 인증을 통해 EU(유럽연합) 27개 회원국에서 닥터눈을 판매·공급할 수 있는 규제 기반을 마련했다. 특히 이번 인증은 까다로운 유럽 MDR 체제 내에서도 사례가 드문 '예측' 목적으로 인증 받았다는 점에서 그 의미가 크다는 설명이다.
메디웨일은 이번 성과가 해외 의료기관 및 파트너사와의 협력 논의에서도 제품 신뢰도를 높이는 계기가 될 것으로 보고 있다. 특히 미국 FDA(식품의약국) 드 노보(De Novo) 절차를 비롯해 다양한 글로벌 규제 전략에 있어서도 속도가 붙을 것이란 기대다.
최태근 메디웨일 대표는 "이번 인증에서 '심혈관 위험 예측'이 닥터눈의 사용 목적으로 명시된 것은 망막 AI 기반 전신 질환 위험 평가라는 차별화된 방향성을 보여주는 중요한 성과"라며 "유럽 현장 적용을 확대하고 파트너십을 강화해 글로벌 확장에 속도를 내겠다"고 했다.
[머니투데이 스타트업 미디어 플랫폼 '유니콘팩토리']
