강한창 약대 교수팀, 암세포 환원 환경서 분해되는 '디셀레나이드 폴리머좀' 설계
화학공학 분야 세계 상위 3% 학술지 'Chemical Engineering Journal' 게재

가톨릭대학교는 최근 강한창 약학대학 교수 연구팀이 암세포의 산화-환원 균형을 파괴하는 동시에 특정 세포소기관을 정밀 타격하는 '차세대 항암 나노플랫폼'을 개발했다고 31일 밝혔다.
일반적으로 약물은 고유 성질에 따라 특정 세포소기관에 축적돼 약효를 발휘한다. 동일한 화학구조의 약물이라도 염(salt)의 유무에 따라 친수성과 소수성이 달라져 다른 세포소기관으로 전달될 수 있다. 하지만 지금까지는 약물 간 세포막 투과성 차이로 인해 세포 내 유입량이 달라지고, 나아가 정밀한 세포소기관을 표적하는 데 한계가 있었다.
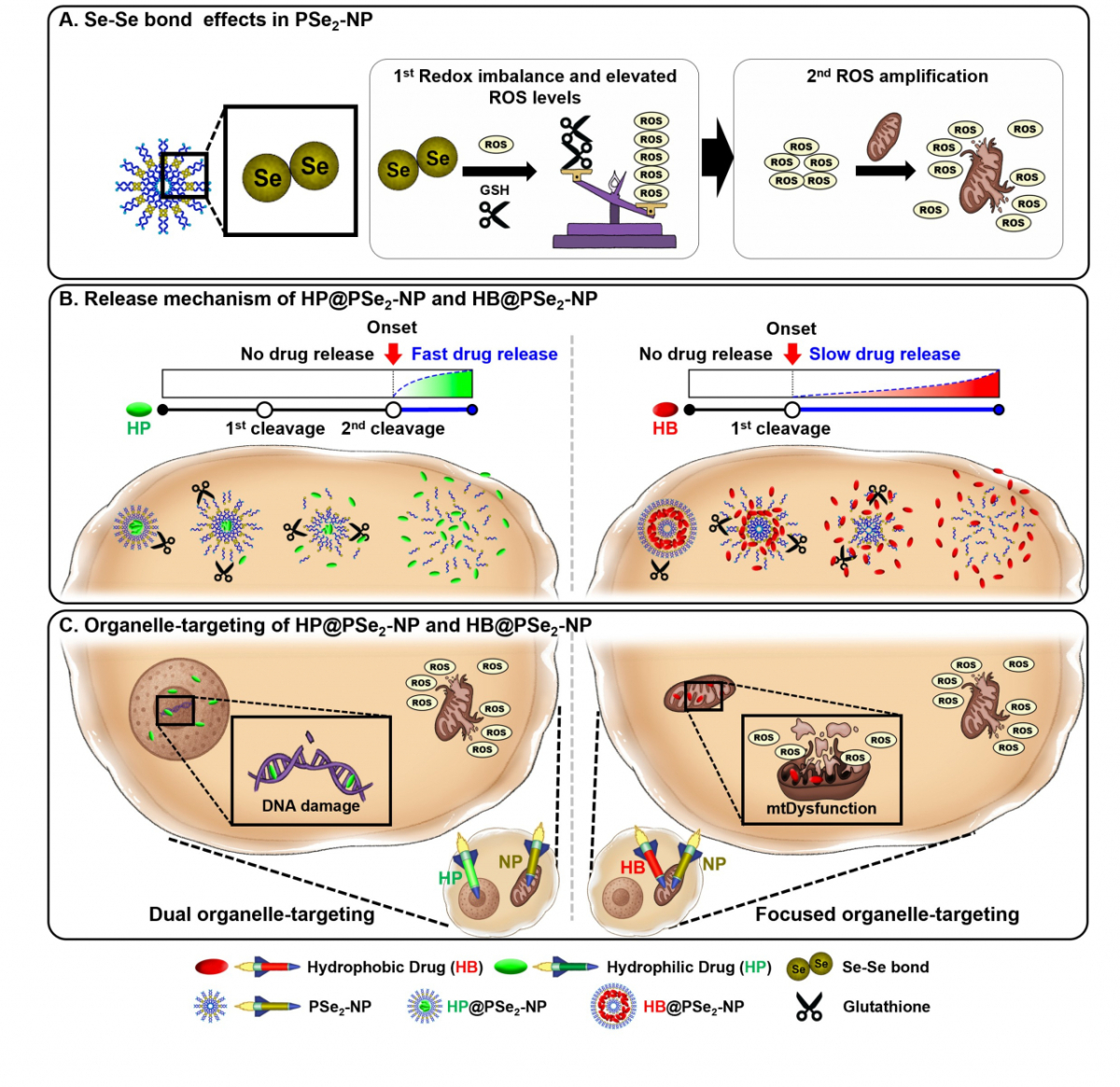
강 교수팀은 암세포의 환원 환경에서 선택적으로 분해되는 디셀레나이드(Se-Se) 폴리머좀(PSe₂-NP) 나노플랫폼을 설계했다. 해당 플랫폼은 친수성 약물은 코어에, 소수성 약물은 막에 각각 탑재해 세포질에서 서로 다른 방출 속도를 구현할 수 있도록 제작됐다.
플랫폼은 항산화 물질인 글루타치온(GSH)을 소모하고 유해 활성산소(ROS)를 증가시켜 암세포의 에너지원인 미토콘드리아의 산화-환원 균형을 선제적으로 파괴한다.
이 과정에서 탑재된 약물에 따라 2가지 정밀한 세포소기관 표적성을 구현한다. 친수성 약물을 탑재한 플랫폼은 미토콘드리아의 산화환원 교란과 핵 DNA 손상을, 소수성 약물을 탑재한 플랫폼은 미토콘드리아의 전자전달계 교란과 기능 손상을 유도한다.
동물 실험 결과, 두 나노 제형은 각각 66%와 62%의 높은 종양 성장 억제율을 기록했다. 특히 약물과 전달체 간의 병용지수(CI) 분석에서 강력한 시너지 효과(CI<1)를 확인했다.
강 교수는 "동일한 화학구조의 약물이라도 극성만 변화시켜 세포소기관 표적성을 조절하고, 나노플랫폼으로 암세포의 생존·사멸 항상성을 동시에 교란하면 약효 시너지를 극대화할 수 있다"며 "질환 맞춤형 차세대 나노플랫폼을 개발하는 후속 연구를 이어갈 것"이라고 전했다.
한편 이번 연구는 과기정통부·한국연구재단, 보건복지부·보건산업진흥원, 교육부·기초과학지원연구원의 지원을 받아 수행됐다. 연구 결과는 화학공학 분야 세계 상위 3% 이내 학술지 'Chemical Engineering Journal'(IF=13.2, JCR Q1)'에 게재됐다.