제넥신(2,990원 ▼20 -0.66%)이 주요 파이프라인 상업화 성과를 확보하는 데 애를 먹고 있다. 중국을 비롯한 아시아 기업과 협업을 토대로 현지에서 다수 임상 연구를 진행했지만, 구체적인 연구 성과로 이어지지 못했다. 제넥신은 중국을 넘어 글로벌 시장으로 사업 영역을 확장하는 동시에 미래성장동력인 TPD(표적 단백질 분해 기술) 파이프라인 고도화를 병행하겠단 목표다.
제넥신은 TPD 파이프라인 폐암 치료제 후보물질 'GX-BP1'의 전임상 결과를 토대로 글로벌 기술이전을 추진하겠다고 16일 밝혔다.
제넥신은 2024년 이피디바이오테라퓨틱스를 흡수합병하면서 차세대 신약 플랫폼 기술로 꼽히는 TPD 연구 역량을 확보했다. 제넥신은 단백질 기반 TPD 기술로 GX-BP1을 비롯해 아토피 피부염 치료제 'GX-BP2' 등을 개발하고 있다.
제넥신은 GX-BP1의 동물실험을 통해 독성과 유효성 평가 등에서 상대적으로 뛰어난 항암 효능을 확인했다고 강조했다. 다른 치료제와 병용요법으로 항암제 내성을 극복할 수 있는 잠재력도 엿봤다. GX-BP1은 암세포의 생존과 전이, 내성 등에 관여하는 'SOX2' 단백질을 공략하는 신약 후보물질이다. SOX2 단백질을 비교적 효과적으로 분해하며 유의미한 수준의 항종양 효과를 나타낸단 설명이다.
제넥신은 오는 17일 미국 샌디에이고에서 열리는 미국암연구학회(AACR 2026)에서 GX-BP1의 전임상 연구 결과를 발표할 예정이다. 제넥신 TPD 파이프라인의 첫 연구 결과 발표로, 이를 토대로 글로벌 기술이전에 적극적으로 나설 계획이다.
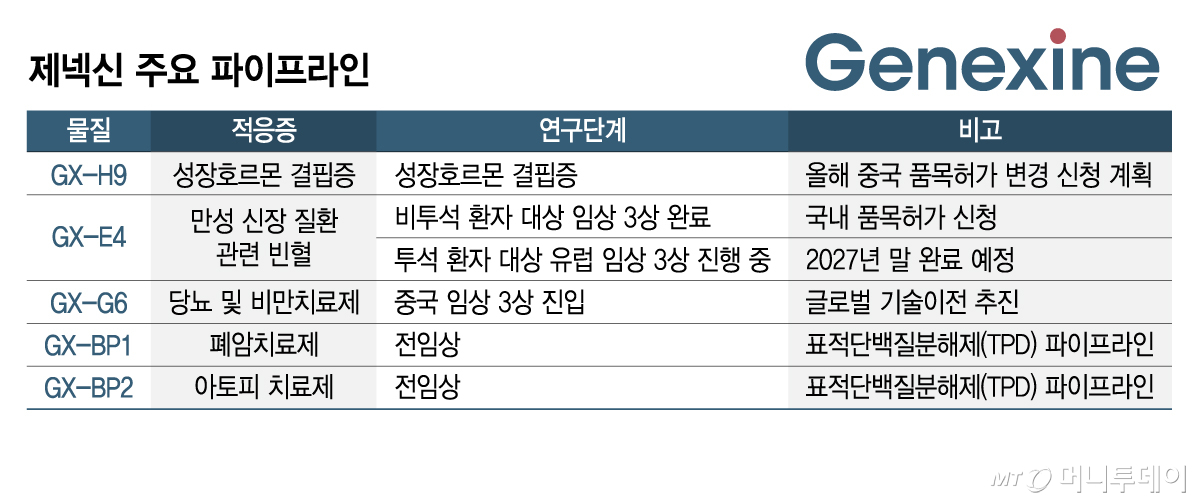
제넥신은 TPD 외 주요 신약 파이프라인의 상업화에도 힘을 쏟고 있다. 소아 대상 성장호르몬 결핍증 치료제(GX-H9)와 만성 신장 질환 관련 빈혈 치료제(GX-E4), 당뇨 및 비만치료제 'GX-G6'의 글로벌 기술이전과 품목허가를 추진하고 있다.
제넥신은 GX-H9의 중국 임상 3상을 완료하고 현지 규제기관에 2024년 12월 품목허가를 신청했지만 아직 허가받지 못했다. 이에 따라 전략을 바꿨다. 정맥주사(IV)가 아닌 피하주사(SC) 제형으로 중국 현지에서 생산하는 약물로 오는 6월 품목허가를 재신청할 예정이다.
제넥신의 GX-E4는 인도네시아에서 비투석 환자를 대상으로 2023년 10월 허가받은 치료제다. 이어 2024년 1월 국내 허가를 신청했다. 현재 규제 기관의 보완 요청에 따라 관련 문서 작업을 진행하고 있다. 이르면 오는 6월 심사 결과가 나올 것으로 예상된다. 이와 별개로 현재 유럽에서 투석 환자 대상 임상 3상을 진행하고 있다.
독자들의 PICK!
제넥신의 GX-G6은 중국 파트너에 기술이전한 뒤 제2형 당뇨와 비만을 적응증으로 임상 2상을 완료하고 임상 3상에 진입했다.
제넥신 관계자는 "기존 주요 파이프라인은 중국을 비롯한 아시아 지역에서 주로 임상시험을 진행하고 품목허가를 꾀했는데, 상업화 과정에서 어려움을 겪은 게 사실"이라며 "중국에서 상업화를 지속 추진하는 동시에 주요 파이프라인을 중국 외 지역으로 확장하기 위한 글로벌 기술이전에 힘쓰고 있다"고 말했다.
또 "특히 제넥신의 미래성장동력이라 할 수 있는 TPD 파이프라인의 전임상에서 좋은 결과를 확인해 고무적"이라며 "AACR 첫 발표를 시작으로 앞으로 1년 안에 TPD 파이프라인의 기술이전에 성공할 수 있게 전사적 역량을 집중하겠다"고 말했다.
