EU, 임상 승인 기간 대폭 단축·특허 인센티브 강화·100억유로 투자 등 다각도로 美·中 추격 나서
中 '임상 속도전'에 유럽도 임상 규정 개편…"한국도 빠른 임상개발 지원해 기술이전 도와야"
유럽연합(EU)이 'EU 바이오기술법' 제정안을 채택하며 글로벌 바이오 경쟁에서 더이상 밀려나지 않겠단 의지를 분명히 했다. 임상시험 승인 기간을 단축하고, 첨단치료의약품(ATMT)에 대한 특허 인센티브까지 담은 이번 법안은 이른바 '임상 리쇼어링'으로 미국은 물론 중국에도 밀린 유럽 신약 연구 분야의 입지를 되찾겠다는 전략으로 읽힌다. 글로벌 기술이전을 전략으로 삼고 있는 한국의 바이오 산업에도 최적화된 경쟁 전략이 뒷받침돼야 한단 지적이 나온다.
25일 업계에 따르면 유럽연합 집행위원회(이하 집행위)는 지난 16일(현지시간) 'EU 바이오기술법' 제정안을 채택했다. 해당 법안은 △임상시험 규정(CTR) 개편 △보충보호증명서(SPC) 개정안 △의약품-의료기기 복합 제품 단일 평가 도입 △EU 위원회와 유럽투자은행그룹(EIBG)의 투자 시범사업 등을 골자로 한다. 집행위는 해당 법안을 내년 3분기에 최종 통과시킬 계획이다.
법안에 담긴 임상시험 규정에 대한 대규모 개편은 임상시험 승인 기간을 대폭 줄이는 것이 핵심이다. 법안에 따르면 다국적(글로벌) 임상시험의 경우 전체 소요 기간이 약 106일에서 75일로, 정보 요청이 없는 경우 75일에서 47일로 단축된다. 또한 첨단치료의약품(ATMT) 임상시험 승인 심사에 적용되는 50일간의 추가 연장도 폐지된다. 이러한 임상시험 승인 절차 간소화는 이르면 내년 1월부터 시범 운영될 예정이다.
집행위는 "유럽은 임상시험 수행에서 상당한 어려움에 직면해 있고, 이는 연구자들의 연구 활동을 저해하고 있다"며 "이러한 장애물에는 길고 복잡한 승인 절차, 자본 접근성의 제한, 미흡한 인프라, 부족한 숙련 인력 등이 포함되며, 이는 결국 환자들이 유망한 신약 치료법을 접하는 것을 지연시키고 있다"고 설명했다.
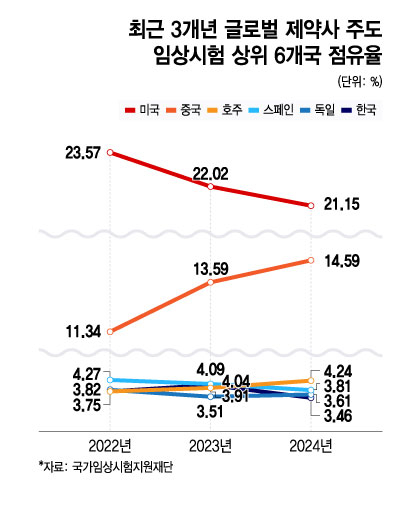
국가임상개발지원재단에 따르면 최근 3년간 글로벌 제약사가 주도한 임상시험이 이뤄진 상위 6개국 점유율은 중국을 중심으로 크게 요동쳤다. 중국의 점유율은 2022년 11.34%에서 지난해 14.59%로 상승한 반면 미국의 점유율은 23.57%에서 지난해 21.15%로 하락했다. 스페인과 독일, 한국 모두 하락세를 보인 가운데 호주만 명확한 상승세를 보여주며 2022년 5위에서 지난해 3위로 올라섰다.
법안엔 유럽에서 개발 및 생산이 이루어진 첨단치료의약품에 대해선 특허 보호 기간을 1년 더 연장받을 수 있게 하는 내용도 포함됐다. 이처럼 임상뿐 아니라 생산까지 포괄하는 조건을 달아 인센티브를 제공하는 건 우호적인 임상 환경이 갖춰진 중국으로 이동한 연구자 및 기업들이 생산까지 중국에서 수행할 것을 우려한 데 따른 것으로 풀이된다.
최근 발효된 미국의 '생물보안법'이 바이오의약품 제조 분야에 초점을 맞춰 중국을 견제한다면 EU의 바이오기술법안은 생산으로 이어지는 길목인 임상 단계의 연구개발(R&D)까지 아우르는 대책이란 평가도 나온다. 미국은 거대한 규모의 의약품 시장을, 유럽은 기초연구부터 R&D, 임상, 상업화에 이르는 신약개발 생태계를 보유하고 있어 각자의 상황에 맞는 전략을 펼치고 있단 분석도 있다.
독자들의 PICK!
이러한 측면에서 한국도 현재의 위치를 고려한 바이오 경쟁 전략을 수립해야 한단 지적이 제기된다. 정부는 최근 바이오시밀러(바이오의약품 복제약) 및 신약 허가 심사 기간을 대폭 단축하겠단 계획을 밝힌 바 있다. 바이오시밀러 개발사와 제네릭(복제약) 기반의 제약사들은 환영하는 분위기지만 일각에선 뜨뜻미지근한 반응도 감지된다. 임상 데이터를 기반으로 글로벌 기술이전을 추진하는 바이오 기업들은 빠른 임상시험 승인이 더 시급하단 입장이어서다.
이승규 한국바이오협회 부회장은 "한국 바이오 산업은 스스로 임상 3상까지 수행하고 허가를 받기엔 아직 자본이나 경험 등 여러가지 측면에서 부족한 상황이라 기술이전을 해야 하는 위치에 있다"며 "글로벌 기술이전으로 하려면 임상 2상 정도의 데이터를 원하기 때문에 그걸 빨리 할 수 있게끔 해줘야 한다"고 말했다.
이어 "신약 인허가 심사 기간을 단축시켜주는 것도 의미가 있지만 그 앞단의 임상시험 허가를 빠르게 해줘서 여러 기업들이 임상 데이터로 글로벌에서 경쟁하게 하는 게 단기적으로 해야 할 일"이라며 "신약을 배출하겠다는 목표에만 집중해서 임상 3상, 인허가 단계만 보고 있어선 안 된다"라고 강조했다.
