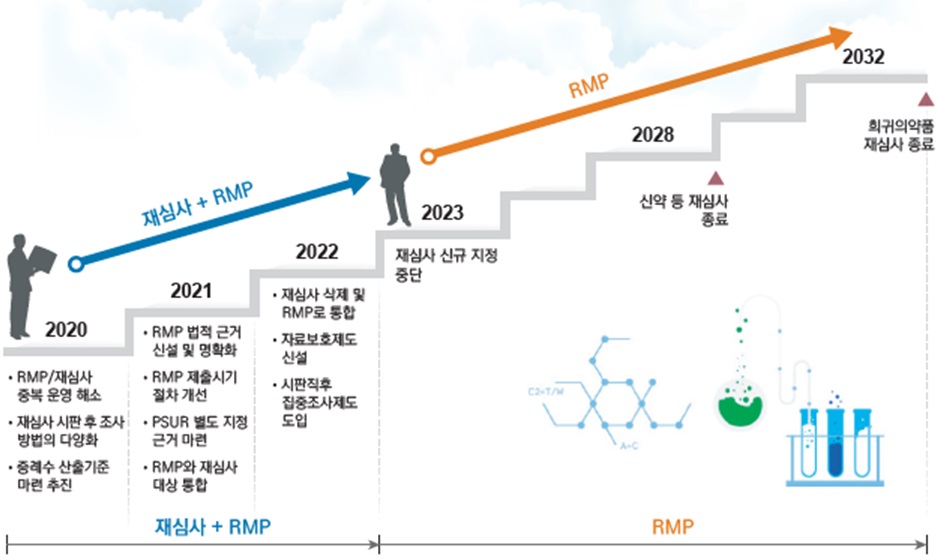
식품의약품안전처가 의약품의 시판 후 안전관리를 위해 각각 운영해온 재심사와 위해성관리계획(RMP·Risk Management Plan) 2개 제도를 앞으로는 RMP 하나로 통합해 운영한다.
16일 식약처에 따르면 의약품 안전관리 제도를 통합 운영하는 것을 골자로 한 ‘의약품 시판 후 안전관리 제도 개선 방안’이 마련됐다. 제도 개선은 3개년에 걸쳐 △올해 제도간 중복 해소 △2021년 RMP 효율성 강화 △2022년 RMP 일원화가 추진된다.
1995년 도입된 ‘재심사’는 신약 또는 일부 전문의약품에 대해 허가 후 일정기간(4~6년) 동안 불특정 다수를 대상으로 부작용 등을 조사해 안전성·유효성을 다시 심사하는 제도다.
2015년 도입된 RMP는 신약 또는 희귀의약품 등에 대해 약물감시계획과 위해성 완화조치방법 등을 포함하는 종합적인 안전관리 계획을 수립해 이행하도록 하는 제도다.
식약처는 “안전관리 대상 의약품이 매년 증가하고 위해성관리계획 품목의 77.5%가 재심사 대상으로도 지정되는 등 자료의 중복제출에 대한 개선과 체계적 관리의 필요성이 제기돼 왔다”고 설명했다.
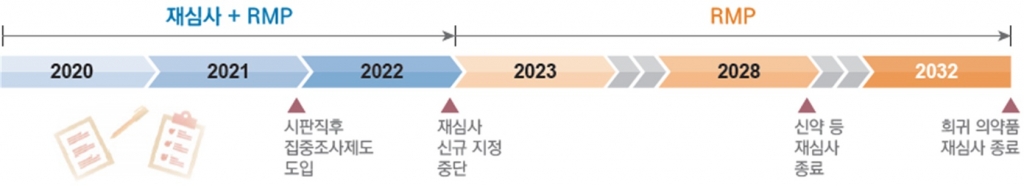
식약처는 이번 제도 개선을 통해 △의약품 시판 후 안전관리 체계의 국제조화 △수집된 안전정보 분석 강화 등 약물감시 내실화 △자료보호제도 신설 등이 이뤄질 것으로 예상했다.
이의경 식약처장은 “의약품 시판 후 안전관리는 허가 당시에는 예상할 수 없었던 의약품의 부작용을 모니터링하고 안전한 의약품 사용을 도움으로써 그 중요성이 높아지고 있다”며 “단계적 개선을 통해 시판 후 안전관리를 강화해 나가겠다”고 밝혔다.
한편 식약처는 식·의약 행정서비스와 관련한 민원이나 제도개선 사항을 국민의 입장에서 발굴하기 위한 ‘제6기 식·의약 옴부즈맨’을 위촉했다.
법률가와 식품·의약품 분야 교수 등 총 5명의 전문가로 구성됐다. 앞으로 2년 동안 △부패 취약분야 및 불합리한 제도 발굴·건의 △민원 불만·불평 해소 등의 역할을 수행한다. 식약처는 이들의 건의사항을 우선 조사해 문제를 해결할 계획이다.
