법적 기한 넘겨 한화케미칼이 허가 신청 자진 취소, 2분기에나 재신청 예정
한화그룹이 추진하고 있는 항체바이오시밀러(바이오복제약) 사업에 빨간불이 켜졌다.한화케미칼(50,200원 ▲850 +1.72%)이 자체 개발 중인 류마티스관절염 항체치료제 'HD 203'(엔브렐의 바이오시밀러)의 판매허가 신청을 자진 취하한 것으로 드러났기 때문이다. 이 바이오시밀러는 세계 시장 규모만 9조원으로 한화케미칼의 바이오복제약 사업에서 큰 상징성을 갖는다. 일부에서는 허가가 늦어져 한화케미칼의 항체치료제 선점효과도 반감될 것으로 보고 있다.
22일 식품의약품안전처 등에 따르면 한화케미칼은 2012년 9월 엔브렐의 바이오시밀러인 HD 203에 대해 판매허가를 식약처에 신청했는데, 법적 허가기간인 2013년 9월까지도 허가를 받지 못해 지난해 9월 허가 신청을 자진 취하한 것으로 뒤늦게 밝혀졌다.
한화케미칼은 허가 신청 자료를 보완해 올 2분기에 HD203의 판매허가를 다시 신청할 계획이다. 한화케미칼 관계자는 "판매허가가 늦어져 전략적으로 자진 취하한 것이 맞다"며 "글로벌 수준에 맞는 허가기준으로 판매허가를 다시 신청해 연내에는 판매허가를 받을 것"이라고 말했다.
HD203은 연 매출 84억달러(9조원) 규모인 와이어스(개발사 암젠)의 항체치료제 엔브렐의 바이오시밀러다. 한화케미칼은 HD203의 세포주 개발부터 배양, 정제, 제형화까지 전 제조 과정을 자력으로 개발했다. 한화케미칼은 국내에서 임상1상과 3상 시험을 각각 마치고, 2012년 9월 식약처에 판매허가를 신청했다.
식약처 관계자는 "한화케미칼 HD203의 경우 안전성과 유효성에서 엔브렐과 동등한 효능은 입증됐다"며 "그러나 기준과 시행방법에 대한 추가 자료를 요청했는데 자료 제출이 늦어져 기한 내에 허가가 이뤄지지 않았다"고 말했다.
이 관계자는 "안전성과 유효성 검토가 끝난 만큼 기준 및 시행방법에 대한 추가 자료 검토가 이뤄지면 판매허가를 내줄 것"이라고 덧붙였다. 기준 및 시험방법은 의약품의 제조방법이 적합한지 평가하는 것이다.
하지만 한화케미칼의 항체바이오시밀러 사업은 큰 차질이 불가피해 보인다. 한화케미칼은 2012년말 글로벌제약사 머크(MSD)로부터 HD203 판매 계약도 해지 당했다. 한화케미칼은 2011년 6월 머크와 7800억원 규모의 항체시밀러 판매계약을 맺었다. 그러나 머크는 사업전략 변경을 이유로 한화케미칼에 계약 해지를 통보했다. 한화케미칼 관계자는 "독자적으로 새로운 판매 파트너를 물색하고 있다"고 말했다.
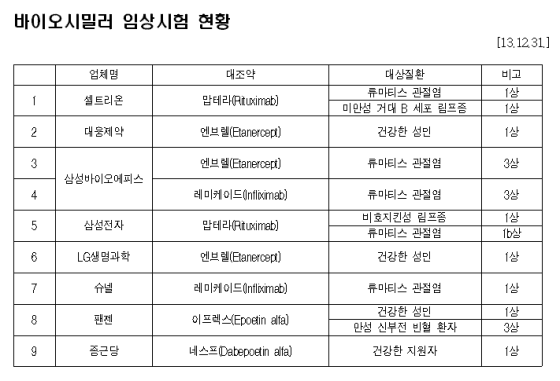
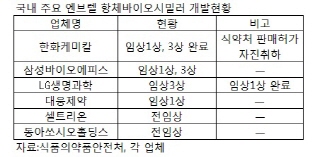
한화케미칼 이외에 현재 엔브렐 항체시밀러를 개발하고 있는 국내 제약바이오 회사는 LG생명과학과 삼성바이오에피스, 대웅제약, 셀트리온, 동아쏘시오홀딩스 등 5개사다. 이중 삼성바이오에피스는 이미 임상3상 시험에 돌입했고, LG생명과학은 임상1상 시험을 지난해 완료했고 현재 임상3상 시험을 준비 중이다. 대웅제약은 임상1상 시험에 돌입했으며, 셀트리온과 동아쏘시오홀딩스는 전임상시험을 진행하고 있다. 이전까지는 한화케미칼이 3~4년 정도 속도가 빨랐지만 지난해 허가 불발로 경쟁사와 개발 격차가 1~2년 정도까지 단축됐다.
독자들의 PICK!
한편 식약처는 지금까지 국내에서 2개의 항체시밀러에 대해 판매허가를 내줬다. 셀트리온이 2012년 7월 레미케이드(존슨앤존슨) 항체시밀러 램시마의 판매 허가를 받았고, 2013년 7월에는 허셉틴(로슈) 항체시밀러도 허가가 났다.