[의료in리포트]
장에서 혈당 배출하는 새 치료 타깃 규명
"새로운 당뇨병 및 체중 감량 치료제 개발 기대"

약물로 비만대사 수술의 혈당 개선 효과를 재현할 수 있는 가능성이 확인됐다.
구철룡 세브란스병원 내분비내과 교수·강찬우 연세의대 내과학교실 교수, 인공지능(AI) 기반 신약 개발 기업 아론티어의 손인석 최고전략책임자(CSO) 연구진은 제2형 당뇨병 치료의 새로운 치료 타깃을 규명했다고 12일 밝혔다. 이를 통해 연구진은 비만대사 수술의 혈당 개선 효과를 약물로 재현할 수 있는 가능성을 확인했다. 연구 결과는 국제학술지 '네이처 커뮤니케이션'(IF 15.7)에 게재됐다.
제2형 당뇨병은 췌장에서 인슐린이 충분히 나오지 않거나 몸에 인슐린 저항성이 생겨 혈당이 높아지는 질환이다. 유전적 요인과 환경적 요인이 복합적으로 작용해 발생하며 국내 당뇨병 환자 대부분이 이에 해당한다.
고도비만인 당뇨병 환자에게 시행되는 비만대사 수술은 치료 효과가 높다. 그러나 수술적 부담과 부작용 우려 등으로 인해 실제 수술률은 대상 환자의 1% 미만에 불과해 적절한 대안이 필요한 상황이다.
연구진은 비만대사 수술 후 관찰되는 또 다른 현상인 '장을 통한 포도당 배출'에 주목했다. 이는 혈액 내 포도당을 장 조직이 흡수한 뒤 이를 다시 장관 내강으로 대변을 통해 배출하는 현상이다. 앞서 연구진은 이 현상을 세계 최초로 제시해 2022년 국가연구개발우수성과 100선에 선정된 바 있다.
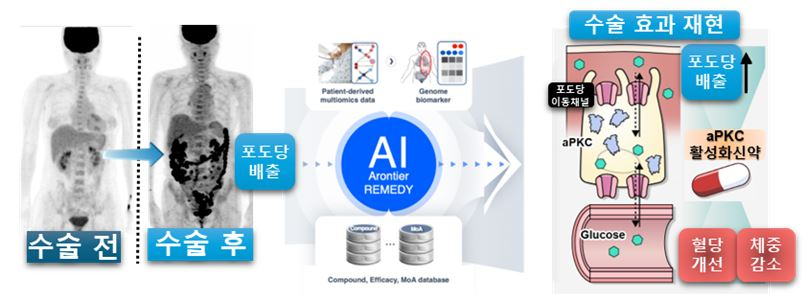
이번 연구에선 혈액 내 포도당을 장관 내로 역배출시키는 핵심 치료 타깃 규명이 주된 과제였다. 연구진은 비만대사 수술을 받은 소장 조직과 다양한 장내 포도당 배출 모델의 전사체 데이터를 통합 분석했다. 또 아론티어의 AI 신약 개발 플랫폼을 활용, 100만건 이상의 유전자 발현 데이터를 비교·분석해 일반 장 조직을 포도당 배설형 조직으로 전환하는 핵심 인자를 탐색했다.
그 결과 단백질 인산화효소 C(PKC)의 활성화 패턴이 포도당 배출 상태에서 나타나는 유전자 발현 변화와 높은 연관성을 보이는 것으로 확인됐다. PKC는 세포의 분화·성장·유전자 발현·사멸 등에 관여하는 신호전달 매개 효소다. 특히 여러 PKC 아형 중에서도 비정형 PKC가 포도당 수송체 1(GLUT1)을 매개로 장내 포도당 배출을 촉진하는 것으로 나타났다.
연구진은 "당뇨병 쥐 모델을 이용해 장 조직의 비정형 PKC를 선택적으로 활성화한 결과에서도 혈액 내 포도당이 장 상피세포를 거쳐 장관 내강으로 배출되는 현상이 증가했다"며 "이에 따라 혈당이 개선되는 효과가 관찰됐다"고 설명했다. AI 기반 신약 개발 플랫폼을 통해 도출된 후보 물질 '프로스타틴'(Prostatin)이 비정형 PKC를 활성화하고 동일한 장내 포도당 배출 기전을 극대화한단 점도 확인됐다.
구철룡 교수는 "비만대사 수술 이후 혈당이 개선되는 기전 중 하나인 장내 포도당 배출을 극대화할 수 있는 새로운 치료 타깃을 규명했다"며 "비만대사 수술의 혈당 개선 효과를 설명하는 분자생물학적 근거를 제공하고, 해당 신호 경로를 표적으로 하는 새 당뇨병 및 체중 감량 치료 전략 개발의 가능성을 제시한단 점에서 큰 의미"라고 말했다.
독자들의 PICK!
한편 이번 연구는 보건복지부가 주관하는 연구중심병원 한미혁신성과창출 연구·개발(R&D) 사업의 지원을 받아 수행됐다.
