정부 '지정기준' 확대
상업화 가시권 '바이젠셀·셀비온·큐로셀' 주목
국내에서도 최근 개발단계 희귀의약품 지정기준 확대 등으로 치료제 개발을 촉진하는 제도가 강화되면서 기술 중심의 바이오텍들에 기회가 확대될 전망이다. 큐로셀, 셀비온, 바이젠셀 등 이미 개발단계 희귀의약품으로 지정된 파이프라인(신약후보물질)을 개발하던 기업들이 상업화를 앞둬 국내 희귀질환 치료제 개발성과도 가시화된다.
26일 업계에 따르면 식품의약품안전처가 지난 3일 공고한 개발단계 희귀의약품은 76개다. 그중 상업화를 앞둔 파이프라인은 △바이젠셀의 NK(자연살해)/T세포 림프종 치료제 'VT-EBV-N' △셀비온의 전립선암 방사성의약품(RPT) '177Lu-DGUL'(포큐보타이드) △큐로셀의 재발성 불응성 거대 B세포 림프종 CAR-T 치료제 '안발셀' 등이다. 가장 최근에 임상2상이 종료된 VT-EBV-N은 하반기 조건부 품목허가 신청에 앞서 중국지역을 중심으로 한 글로벌 기술이전 추진에 속도를 낸다. 임상2상 투여군에서 1차 유효성 평가기준인 2년 DFS(무질병생존비율)가 95%로 확인되는 고무적 결과가 확인되면서다. 국내 판권은 보령이 확보하고 있어 상업화도 빠르게 이뤄질 것으로 전망된다.
지난 2일부터 시행된 희귀의약품 지정에 관한 규정 개정으로 희귀의약품(개발단계 희귀의약품 포함)의 지정기준이 이전보다 명확해지고 적용범위도 확대됐다. 식약처 관계자는 "개정을 통해 개발단계부터 지정에 대한 업체의 예측 가능성을 높이고 제도 운영의 투명성과 공정성을 제고함으로써 희귀의약품 개발촉진과 산업경쟁력 강화가 기대된다"고 말했다.
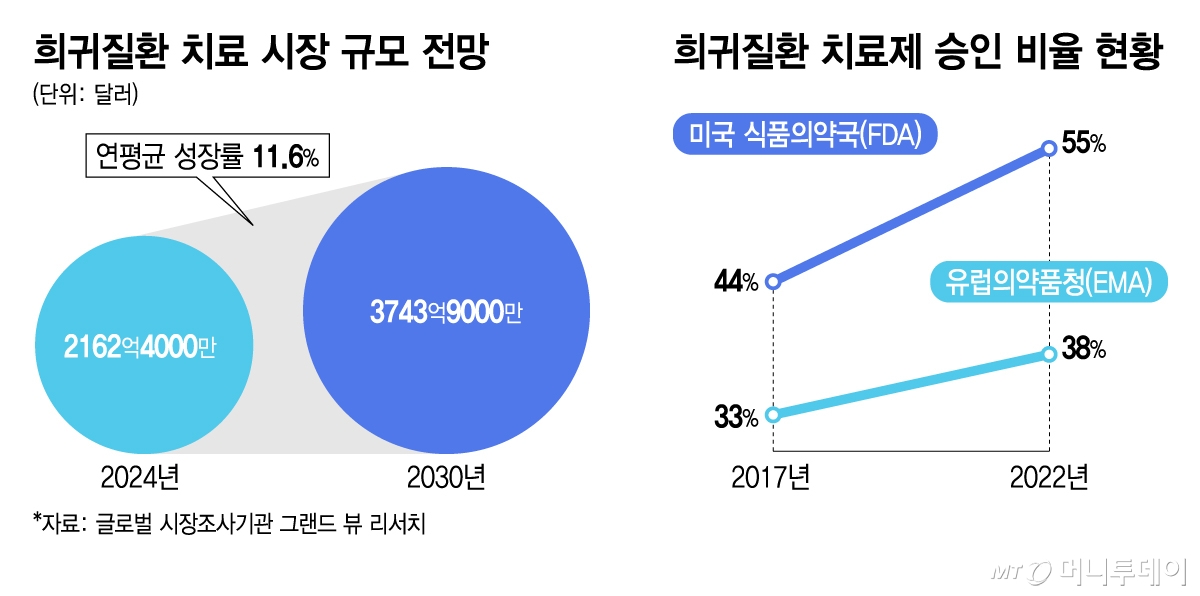
글로벌 시장조사기관 그랜드뷰리서치에 따르면 글로벌 희귀질환 치료시장 규모는 2024년 2162억4000만달러에서 2030년 3743억9000만달러로 연평균 약 11.6% 성장할 것으로 전망된다.
