DLBCL치료 병용 1b상서
객관적반응률 100% 눈길
1차 치료제 진입 기대감↑
리가켐바이오와 에이비엘바이오가 공동개발해 중국 시스톤파마슈티컬스(이하 시스톤)에 기술이전한 ADC(항체-약물접합체) 파이프라인(신약후보물질) 'CS5001'(LCB71·ABL202)의 임상개발이 순항 중이다.
연내 발표될 안전성 데이터를 통해 '베스트 인 클래스'(계열 내 최고) 지위를 확고히 하고 고형암 임상으로 파이프라인의 가치를 극대화할지 주목된다.
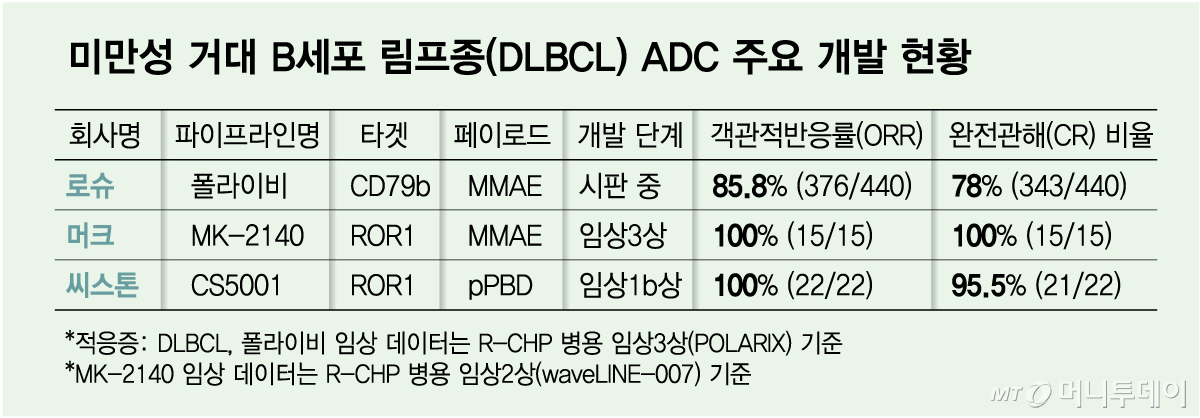
29일 업계에 따르면 시스톤은 지난 26일 ROR1(수용체 티로신키나제 유사 고아 수용체1) 타깃 ADC 파이프라인 CS5001의 글로벌 임상1b상의 현황을 업데이트했다. 1차 DLBCL(미만성 거대 B세포 림프종) 치료에서 CS5001과 표준요법 'R-CHOP'(리툭시맙·사이클로포스파미드·독소루비신·빈크리스틴·프레드니손)를 병용했을 때 ORR(객관적반응률) 100%, CR(완전관해율) 95.5%로 나타났다.
리가켐바이오는 "현재 상업화 또는 후기임상 중인 경쟁약물 대비 높은 효능과 더불어 우수한 안전성을 바탕으로 혈액암 내 가장 큰 시장을 차지하는 DLBCL 1차 치료제 시장에 진입할 가능성이 높아졌다는 점에서 중요한 성과"라고 설명했다.
현재 DLBCL을 적응증으로 상업화된 ADC는 △로슈의 '폴라이비' △ADC테라퓨틱스의 '진론타' △다케다의 '애드세트리스' 등이 있다. 이 중 1차 치료제로 승인받은 폴라이비는 CD79b를 타깃하며 MMAE(미세소관 저해제) 계열 페이로드(약물)가 사용됐다. 폴라이비는 'R-CHP'(리툭시맙·사이클로포스파미드·독소루비신·프레드니손) 병용요법 임상3상에서 ORR 85.5%, CR 78%를 나타냈다. 3등급 이상의 TRAE(치료 관련 이상반응)는 60.7%(435명 중 264명)다.
현재 임상3상 중인 MSD(미국 머크)의 ROR1 타깃 ADC 'MK-2140'은 최초의 ROR1 타깃 DLBCL ADC 치료제다. 폴라이비와 같은 MMAE 계열 페이로드를 적용했다. R-CHP와 병용 임상1b/2상에서 임상3상 권장용량투여군(15명) 기준으로 ORR 100%, CR 100%를 확인했다. 3~4등급의 TRAE는 40%다. 모수가 적어 직접비교에 한계가 있지만 안전성과 효능 측면에서 폴라이비와 유의미한 차이를 보였다.
CS5001은 MK-2140과 타깃은 같지만 독성이 더 강한 PBD(피롤로벤조디아제핀) 계열 페이로드를 사용한다. MK-2140과 유사한 효능을 보이면서 더 우수한 안전성 데이터를 확보하면 '베스트 인 클래스'가 될 수 있다.
독자들의 PICK!
일각에선 CS5001의 실제 가치는 고형암 임상데이터에 따라 결정될 것이라는 전망도 나온다.
시스톤은 PD-L1 항체 '세젬리'(성분명 '수제말리맙')와 병용요법 및 단독요법으로 CS5001의 고형암 임상을 진행 중이다.
업계 관계자는"시스톤이 병용요법 임상도 진행하지만 일단 고형암 단독요법 임상결과가 잘 나오는 게 관건"이라고 덧붙였다.
