혁신제품의 신속도입, 현장애로 해소, 글로벌 규제조화 3대 전략 중심 논의
신약품질분과 등 6개 분야, 15개 소분과, 200여명 참여
식품의약품안전처 소속 식품의약품안전평가원이 '의약품심사소통단(CHORUS)'이 올해 활동을 본격적으로 시작한다고 8일 밝혔다.
의약품심사소통단은 국내 제약산업의 성장‧발전을 위해 필요한 민‧관 공통 아젠다에 대해 선제적이고 실효성 있는 양방향 소통을 위한 민·관 소통채널이다. 올해 혁신제품 신속도입, 현장애로 해소, 글로벌 규제조화의 3대 전략을 중심으로 논의한다.
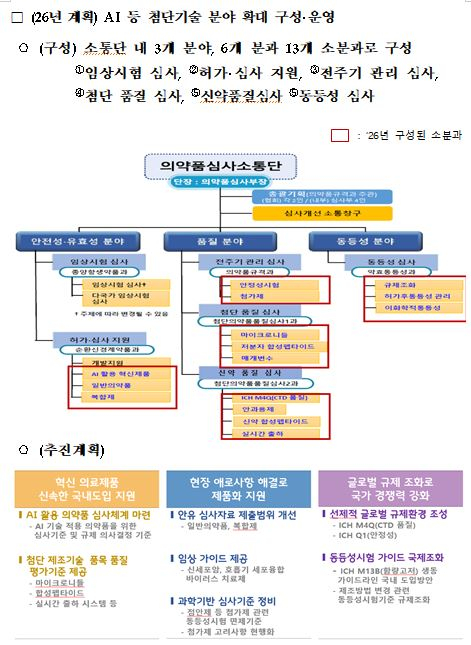
신약심사 혁신방안 추진을 계기로 신약 품질관련 안건을 논의하는 '신약품질심사' 분과를 새롭게 개설한다. 'AI(인공지능) 신약개발협의회' 등 전문가 등 참여 대상을 확대해 6분야 15개 소분과 200여명으로 구성‧운영한다.
의약품심사소통단은 올해 △혁신 의료제품의 허가 지원을 위해 AI(인공지능) 활용한 의약품 심사체계 마련 △첨단 제조기술 품목의 품질 평가기준 제공 △현장 밀착형 규제혁신을 위해 일반의약품 심사자료 개선안 도출 △점안제 등 첨가제 관련 동등성시험 면제기준 정비 △ICH(국제 의약품 규제조화 위원회)의 품질(M4Q) 및 안정성(Q1) 가이드라인 개정 등을 추진한다.
또 올해 식품의약품안전평가원이 새롭게 추진하는 '의약품 신속개발 지원을 위한 가이드라인 사업'에 현장의견을 적극 반영해 과학적이고 합리적인 가이드라인이 개발될 수 있도록 지원도 아끼지 않을 예정이다.
참고로 지난해 의약품심사소통단은 협의체 운영을 통해 식의약 안심 50대 과제인 '의약품 제조소 이전 시 제출자료 합리화' 과제를 발굴했다. '항암제 임상시험 대상자 선정 및 용량 최적화 전략 가이드라인' 등 총 23건의 지침을 제·개정하는 등 실질적인 제약산업 지원 성과를 거뒀다.
식약처는 "앞으로도 현장과 함께 소통하며 규제를 만들고 규제의 투명성과 적용성을 높여 우리 제약산업이 글로벌시장에서 경쟁력을 확보할 수 있도록 지원하겠다"고 강조했다.
